Noch immer ist die Chance, eine im höheren Lebensalter diagnostizierte AML zu überleben, schlecht. Daten aus den USA belegen, dass für Patientinnen und Patienten in der Altersgruppe von 60 bis 69 Jahren, die zwischen 2010 und 2017 behandelt wurden, die Überlebensrate nach fünf Jahren nur 22 Prozent beträgt, für über 70-Jährige liegt sie bei 5 Prozent. Neue Therapien für AML werden deshalb dringend benötigt.
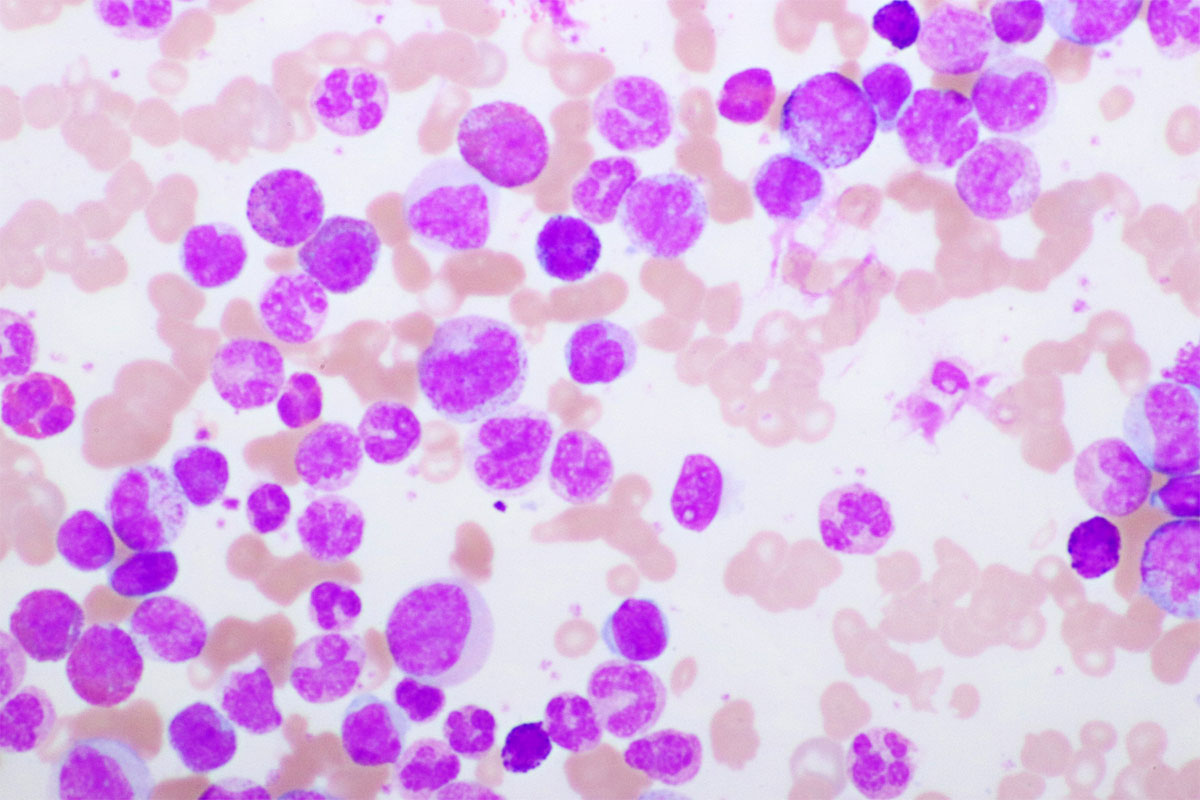
Einen möglichen Ansatz dafür haben die Ulmer Wissenschaftlerinnen und Wissenschaftler in der Funktion des Proteins PIWIL4 gefunden. „Unsere Forschung zeigt, dass PIWIL4 eine entscheidende Rolle für das Überleben und Wachstum von AML-Zellen spielt, während gesunde Blutzellen darauf verzichten können“, erklärt Erstautor Dr. Shiva Bamezai vom Institut für Experimentelle Tumorforschung am Universitätsklinikum Ulm.
Abbau von R-Loops
Das Forschungsteam konnte erstmals nachweisen, dass PIWIL4 als Enzym fungieren und so genannte R-Loops in den AML-Zellen abbauen kann. R-Loops sind dreisträngige Nukleinsäurestrukturen, die während der Transkription von DNA in RNA entstehen können. Sie können die DNA schädigen und sogar zum Zelltod führen. Wenn nicht genügend abbauende Enzyme zur Verfügung stehen, häufen sich solche R-Loops an und blockieren die DNA-Replikation und Transkription in den Krebszellen. „Durch den R-Loop-Abbau ermöglicht PIWIL4 das ungehinderte Wachstum der Leukämiezellen“, ergänzt Bamezai.
Die gezielte Blockade von PIWIL4 führte im Experiment zu einem vermehrten Absterben der AML-Zellen durch R-Loop-Akkumulation. Um diese Schäden zu reparieren, sind die AML-Zellen auf den so genannten ATR-Signalweg angewiesen – und dieser kann durch Medikamente unterdrückt werden.
Krebszellen gezielt schwächen
„Wir konnten einen Ansatzpunkt aufzeigen, um die Krebszellen gezielt zu schwächen, indem wir den R-Loop blockieren“, fasst Professor Christian Buske zusammen. Der Ärztliche Direktor des Instituts für Experimentelle Tumorforschung hat für die Studie zusammen mit Professor Vijay Rawat ein internationales Team koordiniert. Wie bereits eine frühere Studie im Mausmodell zeigte, ist PIWIL4 für gesunde Blutzellen verzichtbar, seine Blockade schadet ihnen also nicht.
Die Forscherinnen und Forscher arbeiteten mit mehreren Partnern zusammen, unter anderem mit der Core Unit Massenspektrometrie und Proteomics der Uni Ulm, die modernste Proteomforschung zur Identifizierung und Quantifizierung von Proteinen anbietet. Auch mit der Harvard Medical School in den USA gab es eine Kooperation. Die Studie wurde von der Deutschen Forschungsgemeinschaft gefördert.
Quelle: Universität Ulm
Originalpublikation: Shiva Bamezai et al.; A noncanonical enzymatic function of PIWIL4 maintains genomic integrity and leukemic growth in AML; Blood, 2023, DOI: 10.1182/blood.2022018651