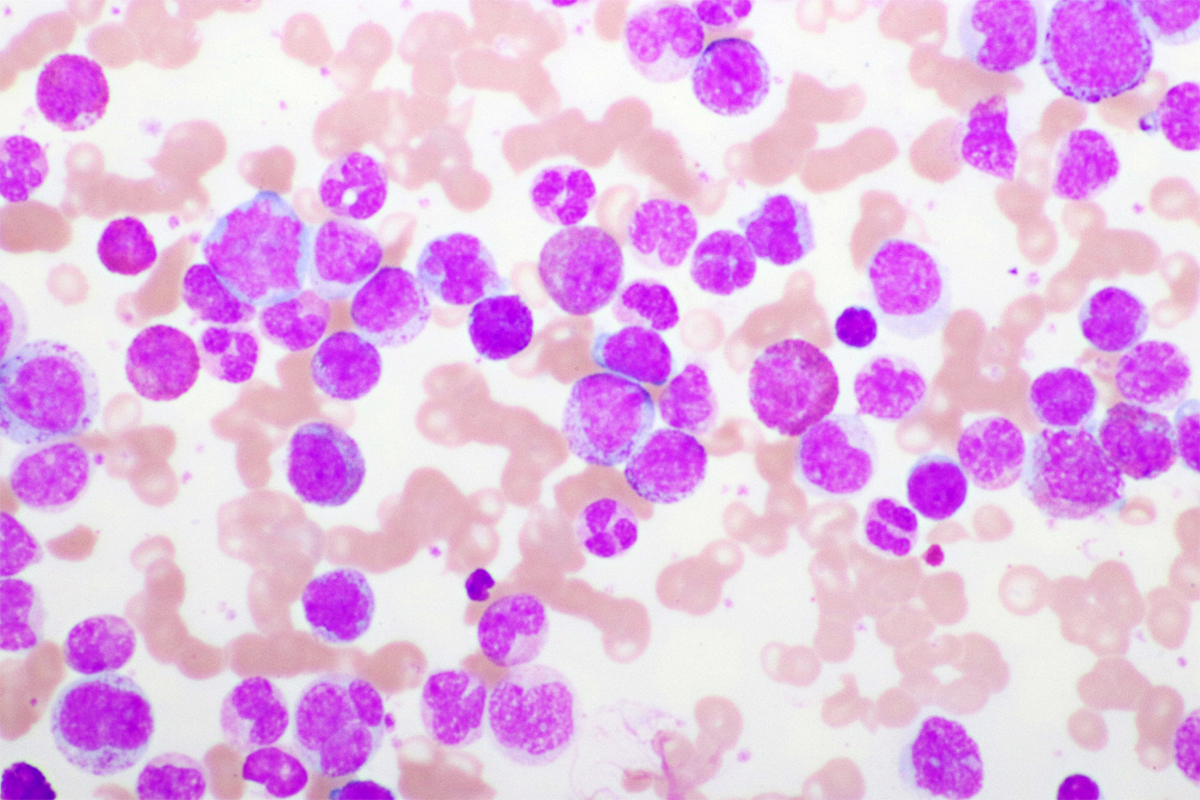
Wissenschaftlerinnen und Wissenschaftler um Prof. Stefan Müller vom Institut für Biochemie II der Goethe-Universität haben in einer aktuellen Arbeit eine bestimmte Blutkrebs-Form untersucht, die akute myeloische Leukämie, abgekürzt AML. Die Erkrankung tritt vor allem im Erwachsenenalter auf und endet bei älteren Betroffenen oft tödlich. Bei einem Drittel der AML-Patientinnen und -Patienten weisen die Krebszellen eine charakteristische Veränderung ihres Erbguts auf. Diese Mutation betrifft das sogenannte NPM1-Gen, das die Bauanleitung für ein Protein gleichen Namens enthält.
Es war bereits bekannt, dass die mutierte NPM1-Variante (Kürzel: NPM1c) ein wichtiger Faktor für die Entstehung von Leukämie ist. „Wir haben nun aber mit einem interdisziplinären Team verschiedener Arbeitsgruppen der Goethe Universität einen neuen Weg entdeckt, wie die NPM1c-Genvariante dies macht“, erklärt Müller. Demnach greift das veränderte Protein in einen wichtigen Zellprozess ein, die Autophagozytose.
Produktion der Autophagosomen
Dabei handelt es sich um einen Stoffwechselweg, über den die Zelle eigene Strukturen recycelt. Diese „Selbstverdauung“ dient einerseits der Beseitigung defekter Moleküle. „Außerdem kann die Zelle so ihren Bedarf an wichtigen Bausteinen decken, etwa bei Nährstoffmangel oder bei erhöhter Zellteilung, einem Charakteristikum von Krebszellen“, erklärt Hannah Mende, Doktorandin und Erstautorin der Studie.
Bei der Autophagozytose erzeugt die Zelle zunächst eine Art Müllbeutel, das Autophagosom. Darin verpackt sie die zellulären Bestandteile, die zerlegt und gegebenenfalls wiederverwertet werden sollen. Der Müllbeutel wird dann zum Wertstoffhof der Zelle transportiert, dem sogenannten Lysosom. Mit Hilfe von Säure und Enzymen wird dort der Beutelinhalt abgebaut. Danach werden die Bausteine in die Zelle entlassen, wo sie wiederverwendet werden können. „Wir konnten nun zeigen, dass NPM1c sowohl die Produktion der Autophagosomen als auch die der Lysosomen fördert“, sagt Müller.
Bindung von NPM1c und GABARAP
Die Forscherinnen und Forscher haben auch aufgeklärt, wie NPM1c diese Effekte vermittelt: Es bindet an einen zentralen Regulator des Autophagosomen-Lysosomen-Systems namens GABARAP und aktiviert ihn dadurch. „Wir haben mit Hilfe von Computersimulationen gezeigt, dass diese Bindung von NPM1c und GABARAP eine untypische Struktur aufweist“, erklärt Ko-Autor Dr. Ramachandra M. Bhaskara, der die Arbeitsgruppe „Computational Cell Biology“ am Institut für Biochemie II leitet.
Experimentelle strukturbiologische Daten bestätigen die Ergebnisse der Simulation. Auf Basis dieser Ergebnisse lassen sich nun möglicherweise Wirkstoffe entwickeln, die ganz spezifisch die Bindung von NPM1c an GABARAP beeinflussen, und damit das Wachstum von Leukämiezellen bekämpfen.
Quelle: Goethe-Universität Frankfurt am Main
Originalpublikation: Hannah Mende et al.; An atypical GABARAP binding module drives the pro-autophagic potential of the AML-associated NPM1c variant; Cell Reports, 2023, DOI: 10.1016/j.celrep.2023.113484