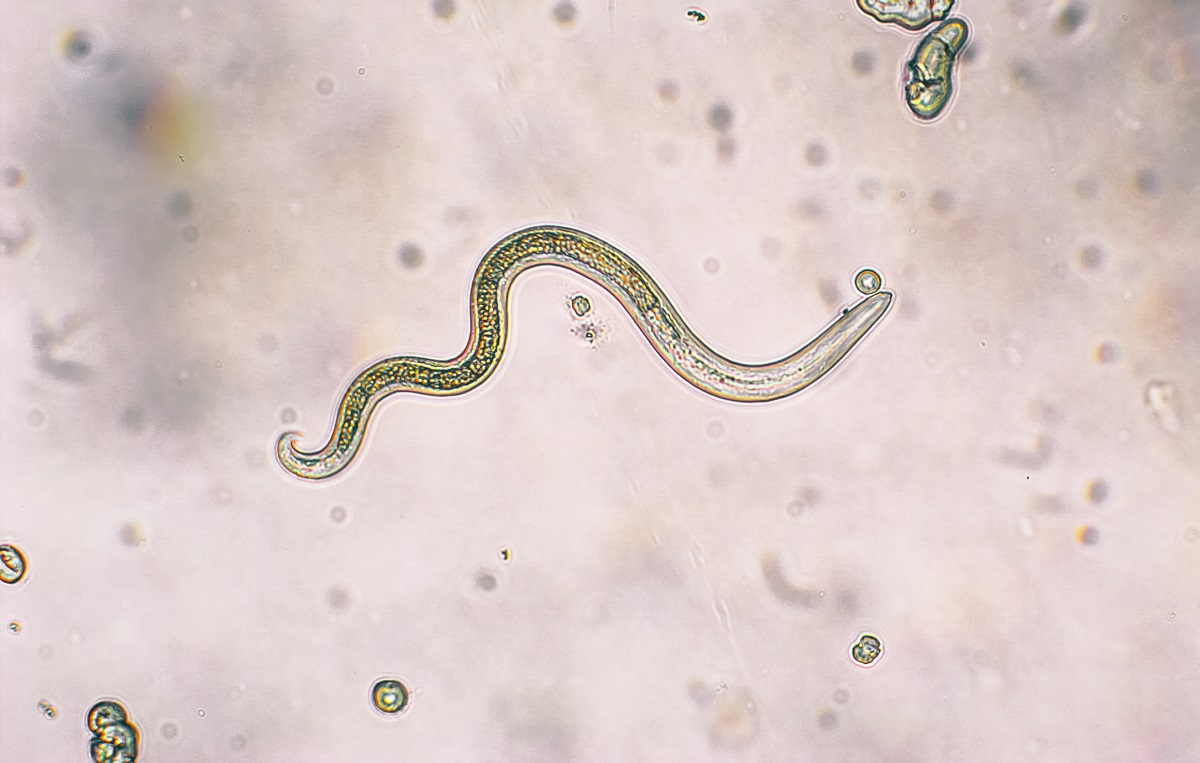
Filarien, schlanke aber mitunter bis zu 70 Zentimeter lange Fadenwürmer, können sich hartnäckig in ihren Wirt einnisten und zu ernsten Infektionskrankheiten in den Tropen führen. Meist sind es Mücken, die die winzigen Larven der Würmer von Mensch zu Mensch übertragen, durch Stechen nehmen sie die Larven aus dem Blut oder der Unterhaut auf und setzen sie in den Gefäßen oder Geweben ihres nächsten Opfers ab.
Wissenschaftler unter Federführung der Universität Bonn haben jetzt einen Mechanismus erforscht, mit dem das Immunsystem den Filarien zu Leibe rückt. Bestimmte Immunzellen, die Eosinophilen Granulozyten, setzen dabei DNA frei, die eine Art Netz um die Larven bildet und sie einfängt. Darüber hinaus identifizierten die Forscher, welches Protein den Mechanismus „einschaltet“, der sogenannte Dectin-1 Rezeptor.
Schwere Erkrankungen durch Filarien
Zunächst sind sie weniger als einen Millimeter groß und werden daher Mikrofilarien genannt, die Larven, die Fadenwürmer direkt im Gewebe ihres Wirts freisetzen. Um sich weiterzuentwickeln und infektiös zu werden, brauchen sie allerdings die Mithilfe von Mücken. Sie nehmen die Mikrofilarien des Wirts mit der Blutmahlzeit auf. Im Körper des Insekts entwickeln sich die Larven weiter und gelangen beim nächsten Stich wieder zum Menschen. Filarien können schwere Erkrankungen wie die Flussblindheit oder Elefantiasis (extreme Lymphschwellungen in den Beinen und/oder Hoden) hervorrufen, die zu den sogenannten Vernachlässigten Tropenkrankheiten gehören und dort bei etwa 80 Millionen Menschen vorkommen.
Um zu untersuchen, welche Mechanismen das Immunsystem gegen solche Eindringlinge einsetzt, sahen sich die Wissenschaftler in ihrer Studie bestimmte Immunzellen, die Eosinophilen Granulozyten, genauer an. Die Zellen haben ihren Namen aufgrund des roten Farbstoffs Eosin, mit dem sie angefärbt werden können. „Eosinophile Granulozyten sind bekannt dafür, dass sie bei Filarieninfektionen einen schützenden Effekt haben. Der genaue Mechanismus war bislang jedoch nicht bekannt“, sagt Studienleiter Prof. Dr. Marc P. Hübner vom Institut für Medizinische Mikrobiologie, Immunologie und Parasitologie am Universitätsklinikum Bonn und vom Deutschen Zentrum für Infektionsforschung (DZIF).
Molekularbiologische Methoden
Die Forschenden nutzten unter anderem molekularbiologische Methoden und die Immunfluoreszenzmikroskopie, um die auftretende DNA zu bestimmen und zu messen. In Zellkulturen fanden sie heraus, dass die Immunzellen auf die Larven der Fadenwürmer reagierten, die Zellen produzierten DNA, die dann außerhalb der Zelle die Larven wie ein Netz umspannte. Das hatte zur Folge, dass sich die Larven nur noch schlecht oder gar nicht mehr bewegen konnten und dadurch unschädlich gemacht wurden.
Der Mechanismus trat sowohl bei freigesetzten Mikrofilarien (erstes Larvenstadium) als auch bei weiterentwickelten Larven in einem bereits infektiösen Stadium (drittes Larvenstadium) auf. Das könnte die Verbreitung der Parasiten reduzieren, denn die übertragenden Insekten treffen in der Folge weniger Mikrofilarien an. Hinzu kommt, dass die vom Insekt übertragenen infektiösen Larven im Endwirt besser bekämpft werden.
Abbau durch DNA-Netze
Auch in einem darauffolgenden Versuch mit Mäusen bestätigte sich die Beobachtung der Wissenschaftler, dass Mikrofilarien durch DNA-Netze abgebaut werden können. Umgekehrt bildeten sich in Mäusen, denen die Eosinophilen Granulozyten fehlten, keine DNA-Netze gegen die Larven. Der Mechanismus von Immunzellen, solche Netze aus DNA zu entwickeln, nennt sich ETosis, ET steht dabei für extracellular traps, also extrazelluläre Fallen. Der Prozess der ETosis ist schon länger bekannt, wurde bisher aber vor allem in anderen Immunzellen, den Neutrophilen Granulozyten, nachgewiesen.
Aber was lässt die Zellen die Gefahr der Larven erkennen und DNA-Netze freisetzen? Die Wissenschaftler fanden heraus, dass es ein bestimmtes Protein auf der Zelloberfläche ist, der Dectin-1 Rezeptor. Wenn die Zellen in Kontakt mit den Wurmlarven kommen, wird er in Gang gesetzt und löst den Mechanismus aus, bestehend aus einer Reihe aufeinanderfolgender Signale. Aus welchen Teilen der Zelle die freigesetzte DNA stammt, konnten die Wissenschaftler ebenfalls herausfinden: Die primäre Quelle sind die Mitochondrien, die „Kraftwerke“ der Zelle. Aber auch aus dem Zellkern wurde DNA in die Netze eingespeist, freigesetzt durch biochemische Veränderungen.
Konservierter Mechanismus
„Unsere Ergebnisse belegen, dass die Eosinophile ETosis ein konservierter Mechanismus ist. Das zeigt sich daran, dass sowohl menschliche als auch tierische Eosinophile Granulozyten in der Lage sind, ihre DNA freizusetzen, wenn sie in Kontakt mit Filarien verschiedener Spezies kommen“, betont Erstautorin Dr. Alexandra Ehrens von der Universität Bonn. Die Ergebnisse der Studie können zukünftig dazu beitragen, Strategien gegen die Verbreitung von Krankheiten zu finden, die durch Filarien ausgelöst werden. In Folgestudien wollen die Wissenschaftler untersuchen, welche Relevanz der entdeckte Abwehrmechanismus für die Bekämpfung solcher Filariosen in Afrika haben kann.
An der Studie waren neben der Universität Bonn und dem DZIF in Bonn das Muséum National d’Histoire Naturelle in Paris (Frankreich) und das Unternehmen Elanco Animal Health in Monheim beteiligt. Marc Hübner ist auch Mitglied des Transdisziplinären Forschungsbereichs (TRA) „Leben und Gesundheit“ der Universität Bonn.
In sechs verschiedenen TRAs kommen Wissenschaftler aus den unterschiedlichsten Fakultäten und Disziplinen zusammen, um gemeinsam an zukunftsrelevanten Forschungsthemen der Exzellenzuniversität zu arbeiten. Die Studie erhielt finanzielle Unterstützung durch die Deutsche Forschungsgemeinschaft und den durch sie geförderten Exzellenzcluster ImmunoSensation2 der Universität Bonn sowie die Jürgen Manchot Stiftung.
Quelle: Rheinische Friedrich-Wilhelms-Universität Bonn
Originalpublikation: Alexandra Ehrens et al.; Microfilariae Trigger Eosinophil Extracellular DNA Traps in a Dectin-1-Dependent Manner; Cell Reports, 2021, DOI: 10.1016/j.celrep.2020.108621