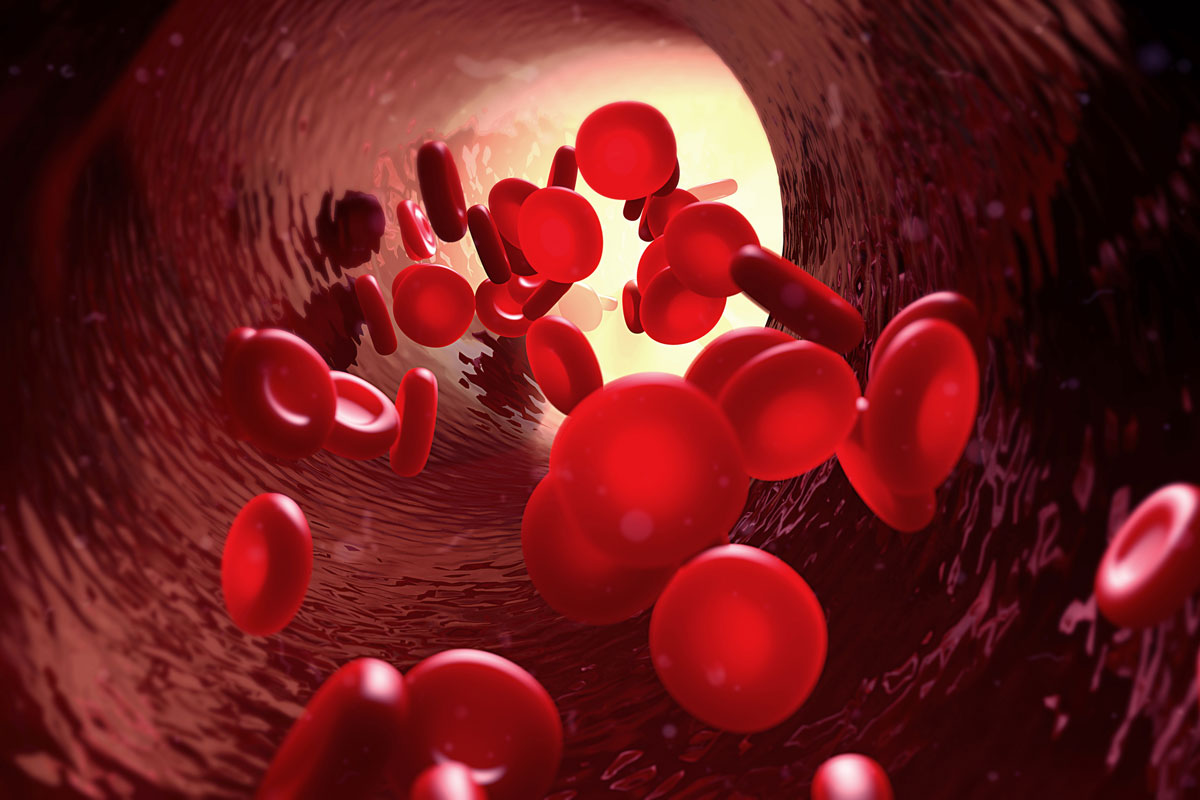
Blutbild bei TTP: Die roten Blutkörperchen wurden an den Blutgerinnseln verletzt (Halbmonde und Fragmente statt runder Blutkörperchen). Die Blutplättchen fehlen fast gänzlich. © Universitätsklinik für Hämatologie, Inselspital, Universitätsspital Bern
Blutbild bei TTP: Die roten Blutkörperchen wurden an den Blutgerinnseln verletzt (Halbmonde und Fragmente statt runder Blutkörperchen). Die Blutplättchen fehlen fast gänzlich. © Universitätsklinik für Hämatologie, Inselspital, Universitätsspital BernBei gesunden Personen spaltet die Eiweißschere ADAMTS13 im Blut das Protein „Von-Willebrand-Faktor" (VWF). Damit wird verhindert, dass Blutplättchen (Thrombozyten) spontan mit dem VWF verkleben und Gerinnsel bilden. Bei der TTP fehlt die ADAMTS13. VWF und Blutplättchen verklumpen, Gerinnsel verstopfen die Gefäße. Dadurch werden die Organe schlechter durchblutet, Herzinfarkt, Hirnschlag und Nierenversagen sind die Folgen.
Die thrombotisch-thrombozytopenische Purpura (TTP) ist eine Autoimmunerkrankung, bei der Autoantikörper den schweren ADAMTS13-Mangel verursachen. Die Standardtherapie besteht bisher aus täglichem Plasmaaustausch (Entfernung der Autoantikörper, Zufuhr von ADAMTS13) in Kombination mit immunsuppressiven Medikamenten (Unterdrückung der Autoantikörperproduktion).
Trotz dieser Behandlung sterben immer noch 10–20 Prozent der Patientinnen und Patienten während eines akuten Schubes. Mehr als die Hälfte der Überlebenden weisen zudem bleibende Organschäden und Einschränkungen auf, vor allem in Form von neurologischen Defiziten, Rückfälle sind häufig.
Eine internationale Studie mit Beteiligung der Universitätsklinik für Hämatologie am Inselspital Bern konnte die Wirksamkeit einer neuartigen TTP-Behandlung, welche die Krankheit innerhalb weniger Tage zurückdrängt und die Organe vor weiterer Minderdurchblutung bewahrt, bestätigen. Dabei verhindert ein gegen den VWF gerichteter Nanobody (Caplacizumab) die Bindung der Blutplättchen an dieses große klebrige Protein und so die Bildung von VWF-Plättchengerinnseln in den kleinen Gefäßen.
Leichte Blutungen traten häufiger auf
An der Phase-III-Studie nahmen 145 Patientinnen und Patienten teil, 72 von ihnen erhielten während der Plasmaaustauschbehandlung und 30 Tage darüber hinaus den Nanobody, 73 gleich lange ein Placebo. Mit dem neuen Wirkstoff endete die Akutphase der TTP für 75 Prozent der Erkrankten bereits nach 2,95 Tagen gegenüber 4,5 Tagen unter der herkömmlichen Therapie.
Zudem benötigten die Patientinnen und Patienten weniger Plasmaaustausche (Median 5 vs. 7) und konnten das Spital früher verlassen. Die Nebenwirkungen der Behandlung waren insgesamt vergleichbar. Erwartungsgemäß traten allerdings unter dem neuen Wirkstoff leichte Blutungen etwas häufiger auf (65 Prozent gegenüber 48 Prozent mit Placebo).
Damit konnten die vielversprechenden Daten aus der Phase-II-Studie, an der die Berner Hämatologie ebenfalls beteiligt war, bestätigt werden. Die Universitätsklinik für Hämatologie am Inselspital und die Universität Bern (Forschungsgruppe Hämatologie, Department for BioMedical Research) erforschen bereits seit Mitte der 1990er Jahre die TTP und ADAMTS13.
Diese Forschung wurde von Prof. em. Dr. phil nat. Miha Furlan und Prof. em. Dr. med. Bernhard Lämmle mit der Entdeckung der „Von-Willebrand-Faktor"-spaltenden Protease und der Beobachtung ihres Fehlens bei der TTP initiiert, und aktuell von Frau Prof. Dr. med. Johanna Kremer Hovinga geleitet. Seit 2010 ist sie an der Entwicklung des neuen Therapieansatzes für TTP beteiligt, der künftig allen TTP-Patientinnen und Patienten zur Verfügung stehen wird.
Quelle: Inselspital, Universitätsspital Bern
Originalpublikation: Marie Scully et al., Caplacizumab Treatment for Acquired Thrombotic Thrombocytopenic Purpura, DOI: 10.1056/NEJMoa1806311