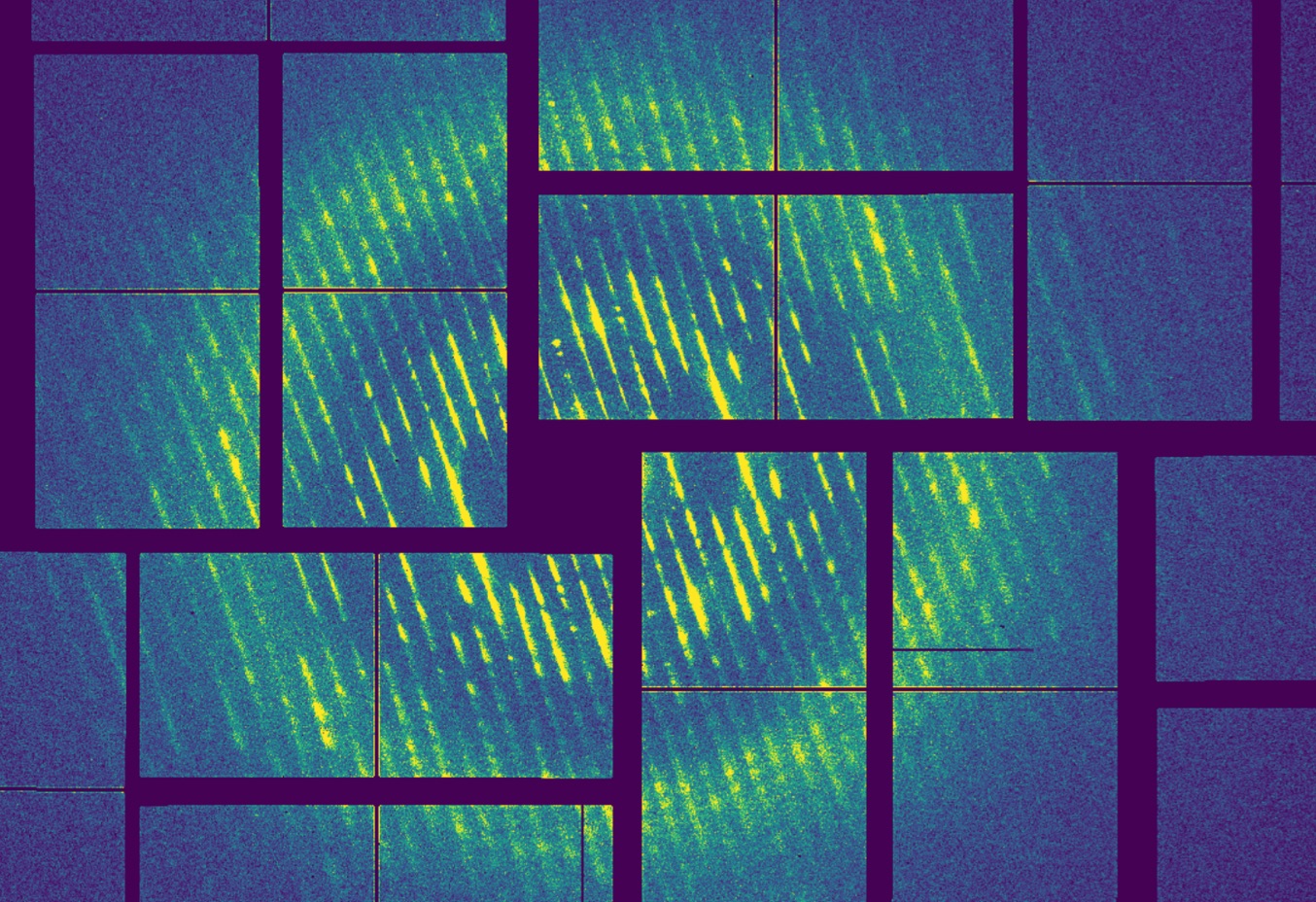
Die Streuung von Röntgenlicht an Amyloidfibrillen liefert ähnliche Muster wie jene, die Rosalind Franklin 1952 von der Erbsubstanz DNS gewann und die schließlich zur Entdeckung der heute wohlbekannten Struktur der Doppelhelix führten.
Der jetzt verwendete Freie-Elektronen-Röntgenlaser LCLS am US-Forschungszentrum SLAC ist allerdings Billionen Mal heller als Franklins Röntgenröhre und ermöglicht, einzelne Amyloidfibrillen zu untersuchen, die Bestandteile der Amyloidfilamente. In dem hellen Röntgenlicht geht das Signal der winzigen Fibrillen allerdings leicht im Streulicht von Umgebungsmaterial unter, etwa der Trägerflüssigkeit für die Proben.
Dieses Problem lösten die Forscher, indem sie ihre Proben auf einem ultradünnen Träger aus Graphen lagerten, einem nur eine Atomlage dicken Film aus Kohlenstoff. Dieser dünne Probenträger streut so wenig, dass sich selbst extrem schwache Signale aufzeichnen lassen.
Immer mehr funktionelle Amyloidformen
Damit bedeutet die Methode auch einen wichtigen Schritt hin zur Untersuchung einzelner Moleküle an Röntgenlasern, ein langgehegtes Ziel der Strukturbiologie. Amyloide sind lange, geordnete Proteinfasern, die aus tausenden identischen Untereinheiten bestehen. Während ihnen eine große Rolle bei der Entstehung neurodegenerativer Krankheiten zugeschrieben wird, finden sich neuerdings immer mehr funktionelle Amyloidformen.
„Das ‚Glückshormon‘ Endorphin beispielsweise kann Amyloidfibrillen in der Hirnanhangsdrüse bilden. Diese lösen sich bei einer Änderung des Säurewerts in seiner Umgebung in einzelne Moleküle auf, die dann ihre Funktion im Körper erfüllen können“, erläutert DESY-Wissenschaftlerin Carolin Seuring vom Center for Free-Electron Laser Science (CFEL), Hauptautorin der Veröffentlichung.
„Andere Amyloide, wie etwa jene, die sich im Hirn von Alzheimer-Patienten finden, sammeln sich im Hirn an und lassen sich nicht auflösen, so dass sie auf Dauer die Hirnfunktion beeinträchtigen.“ Forscher versuchen, die räumliche Struktur von Amyloiden möglichst genau zu bestimmen, um aus diesen Informationen mehr über die Funktions- und Wirkmechanismen der Proteinfasern herauszufinden.
Strukturanalyse von Amyloiden ist kompliziert
„Unser Ziel ist es zu verstehen, welche Rolle die Bildung und Struktur von Amyloidfibrillen im Körper und der Entstehung von neurodegenerativen Krankheiten spielt“, beschreibt Seuring die Motivation „Die Strukturanalyse von Amyloiden ist kompliziert, und Unterschiede zwischen verschiedenen Fasern in einer Messprobe erschweren zusätzlich deren Untersuchung mit den bestehenden Methoden.“
Ein Problem ist, dass sich Amyloide nicht in eine Kristallform züchten lassen, die normalerweise für die Strukturanalyse mit Röntgenlicht nötig ist. Einzelne Amyloidfibrillen sind nur wenige Nanometer breit und damit in der Regel zu klein, um ein messbares Signal im Röntgenlicht zu erzeugen.
Üblicherweise werden daher Millionen der Fibrillen parallel ausgerichtet und gebündelt, damit sich ihre Einzelsignale überlagern und so gegenseitig verstärken. Damit stammen die aufgenommenen Röntgenbeugungsbilder allerdings vom gesamten Ensemble, Information zu Strukturunterschieden zwischen einzelnen Fibrillen gehen verloren.
Amyloide auf hauchdünnem Träger
„Der Großteil unseres Wissens über Amyloidfibrillen stammt aus Untersuchungen per Festkörper-Kernspinresonanz (NMR) und mit Kryo-Elektronenmikroskopen“, erläutert Seuring. „Bei so heterogenen Proben wie den Amyloiden und auch bei der Beobachtung der Dynamik der Fibrillenbildung stoßen die existieren Untersuchungsmethoden jedoch an Grenzen.“
Um in der Zukunft Zugang zu solchen heterogenen Proben zu bekommen, wählte das Team einen neuen Ansatz. Statt in einer Trägerflüssigkeit platzierten die Wissenschaftler die einzelnen Amyloide auf einem hauchdünnen Träger aus Graphen, einer sechseckigen Anordnung von Kohlenstoffatomen, die an eine Art atomare Bienenwaben erinnert.
„Dieser Probenträger hat zwei Vorteile“, betont Forschungsleiter Prof. Henry Chapman vom CFEL, Leitender Wissenschaftler bei DESY. „Zum einen ist Graphen nur eine einzelne Atomlage dünn und hinterlässt daher im Gegensatz zu einer Trägerflüssigkeit kaum eine Spur im Röntgenstreubild. Zum anderen sorgt seine regelmäßige Struktur dafür, dass sich die Proteinfibrillen auf ihm alle in derselben Richtung anlagern, zumindest über größere Bereiche.“
Strukturunterschiede werden deutlich sichtbar
Die Streubilder mehrerer Fibrillen überlagern und verstärken sich dadurch ähnlich wie in einem Kristall, es entsteht jedoch nahezu kein störender Streuhintergrund wie von einer Trägerflüssigkeit. Auf diese Weise ließen sich Streubilder bereits aus weniger als 50 Amyloidfibrillen gewinnen, wodurch Strukturunterschiede deutlicher zutage treten.
„Wir haben charakteristische Asymmetrien in unseren Daten beobachtet, die nahelegen, dass sich mit unserer Technik sogar die Struktur individueller Fibrillen bestimmen lassen könnte“, sagt Seuring. „Das CXI-Instrument am LCLS liefert einen außergewöhnlich hellen, nano-fokussierten Röntgenstrahl, der es uns ermöglicht hat, bereits aus einer derart kleinen Zahl von Fasern Daten zu gewinnen“, berichtet Ko-Autorin Mengning Liang vom SLAC.
„Fibrillen sind damit nach Einzelpartikeln und Kristallen eine dritte Kategorie von Proben, die sich auf diese Weise an Röntgenlasern untersuchen lassen. In gewisser Hinsicht schließen sie eine Lücke zwischen den beiden anderen Probenarten: Sie haben wie Kristalle regelmäßige, sich wiederholende Variationen in ihrer Anordnung, aber nicht deren feste Struktur.“
Bestimmung der kompletten Struktur
Die Forscher testeten ihre Methode mit Proben des Tabak-Mosaikvirus, das ebenfalls Filamente bildet und dessen Struktur heute sehr genau bekannt ist. Tatsächlich lieferte der Test einfache Strukturdaten des Virus mit einer Genauigkeit von 0,27 Nanometern (millionstel Millimetern), das entspricht fast atomarer Auflösung.
Die Untersuchung deutlich kleinerer Amyloid-Fibrillen aus Endorphin sowie aus dem Hormon Bombesin, das unter anderem bei bestimmten Krebsarten eine Rolle spielt, lieferte ebenfalls einige Strukturinformationen, mit einer Genauigkeit von 0,24 Nanometern.
Für die Bestimmung der kompletten Struktur reichten die Daten nicht aus, aber die Studie zeigt, dass die Methode funktioniert und eröffnet damit einen neuen Weg zur Strukturuntersuchung von Amyloiden an Röntgenlasern. „Es ist faszinierend, dass wir sehr ähnliche Experimente durchführen wie Franklin, aber jetzt die Ebene einzelner Moleküle erreichen“, sagt Chapman.
Quelle: Deutsches Elektronen-Synchrotron DESY
Originalpublikation: Henry N. Chapman et al.; Femtosecond X-ray coherent diffraction of aligned amyloid fibrils on low background graphene; Nature Communications, 2018; DOI: 10.1038/s41467-018-04116-9