Im Laufe eines Tages entstehen in jeder Zelle des menschlichen Körpers durch innere und äußere Einflüsse – wie Stoffwechselvorgänge, Entzündungsreaktionen, Umweltgifte und Strahlung – tausende von Schäden der Erbsubstanz (DNA). Falls diese nicht rechtzeitig von der Zelle „repariert“ werden, können sie zu Mutationen und zur Krebsentstehung führen. Besteht die Gefahr, dass sich eine Körperzelle in eine Krebszelle verwandelt, wird normalerweise das Protein p53 aktiviert.
p53 setzt daraufhin mehrere molekulare Prozesse in Gang, die die Zellteilung anhalten („Zellzyklus-Arrest“) und die Genauigkeit der DNA-Reparatur verbessern. „Hierdurch gewinnt die Zelle Zeit, um die gefährlichen DNA-Schäden sauber zu reparieren oder, falls es zu viele sind, den ‚programmierten Zelltod‘ (‚Apoptose‘) einzuleiten“, schildert der Konstanzer Toxikologe und Biochemiker Dr. Aswin Mangerich, der das Projekt an der Professur für Molekulare Toxikologie von Prof. Dr. Alexander Bürkle an der Universität Konstanz leitet.
„Auf diese Weise wirkt p53 der Krebsentstehung entgegen und wird daher auch als ‚Wächter des Genoms‘ (‚Guardian of the Genome‘) bezeichnet“, führt Mangerich weiter aus. Die biomedizinische Relevanz des Proteins p53 wird darin deutlich, dass in der Hälfte aller menschlichen Tumorarten das p53-Gen mutiert (irreversibel verändert) ist, wodurch seine krebsbekämpfende Funktion unterdrückt wird.
„Wächter“ und „Hausmeister“ tun sich zusammen
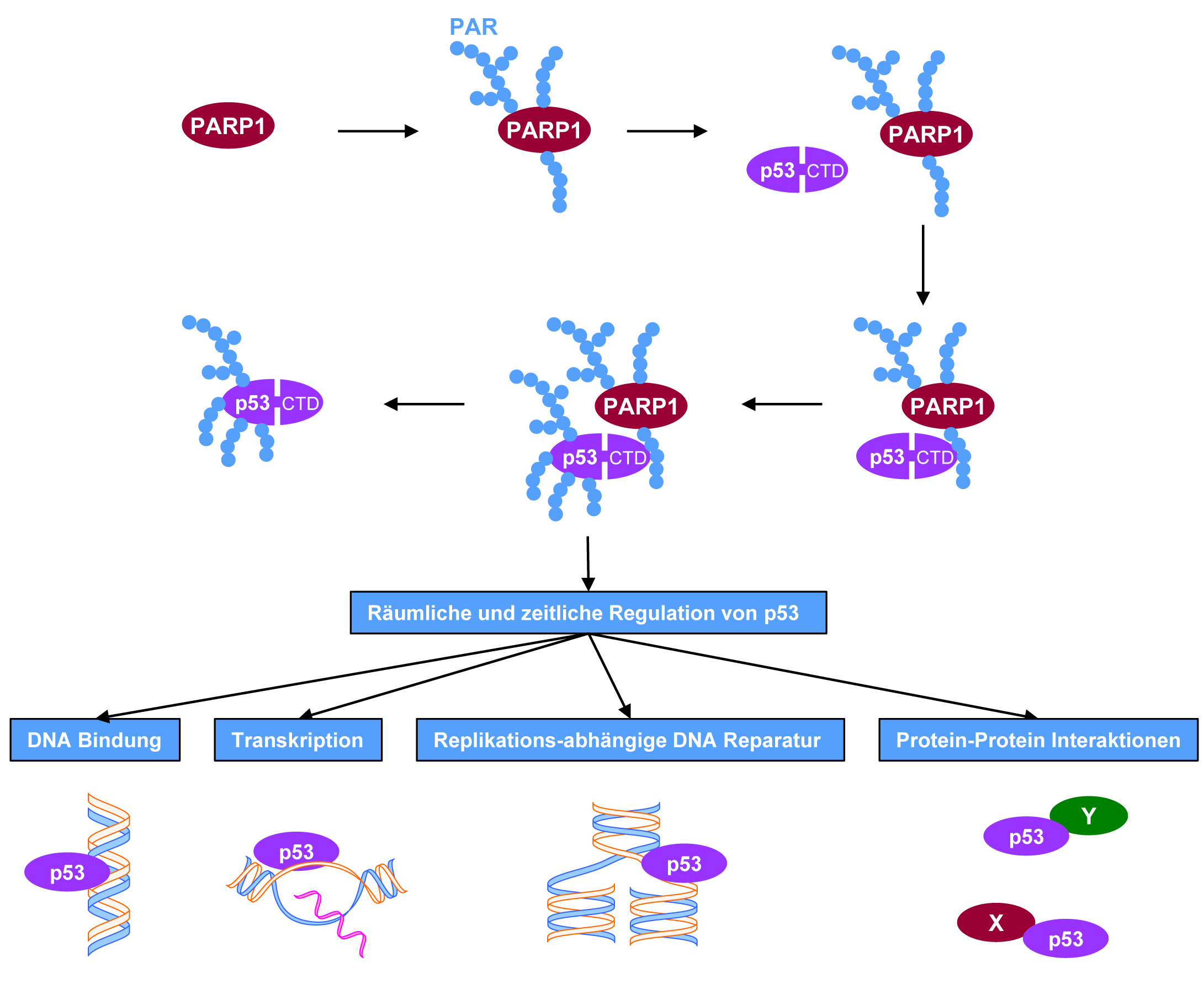 Ein molekularer Mechanismus aufgeschlüsselt: Das Enzym PARP-1 bildet nach Aktivierung (z. B. durch DNA-Schäden) das Biopolymer PAR (Poly(ADP-Ribose)). PAR vermittelt daraufhin die Bindung an das krebsbekämpfende Protein p53, im Bereich der sogenannten C-terminalen Domäne (CTD). p53 wird anschließend von PARP-1 mit dem PAR-Biopolymer modifiziert. Wie im unteren Teil der Abbildung dargestellt, haben diese molekularen Vorgänge weitreichende Auswirkungen auf eine ganze Reihe biochemischer und zellulärer Funktionen, die eine wichtige Rolle in der Krebsbiologie spielen. © Aswin Mangerich / Universität Konstanz
Ein molekularer Mechanismus aufgeschlüsselt: Das Enzym PARP-1 bildet nach Aktivierung (z. B. durch DNA-Schäden) das Biopolymer PAR (Poly(ADP-Ribose)). PAR vermittelt daraufhin die Bindung an das krebsbekämpfende Protein p53, im Bereich der sogenannten C-terminalen Domäne (CTD). p53 wird anschließend von PARP-1 mit dem PAR-Biopolymer modifiziert. Wie im unteren Teil der Abbildung dargestellt, haben diese molekularen Vorgänge weitreichende Auswirkungen auf eine ganze Reihe biochemischer und zellulärer Funktionen, die eine wichtige Rolle in der Krebsbiologie spielen. © Aswin Mangerich / Universität KonstanzDurch diese Mutationen erhalten Krebszellen einen Überlebensvorteil, da die wichtigen Abwehrmechanismen der DNA-Reparatur und des programmierten Zelltods ausgeschaltet werden. Die Konstanzer Wissenschaftler ermittelten nun den molekularen Mechanismus, wie die biochemischen und zellulären Funktionen von p53 in Zusammenspiel mit dem Enzym PARP-1 gesteuert werden.
„PARP-1 hilft dabei, DNA-Reparaturvorgänge in der Zelle zu koordinieren, und wird daher auch als ‚Hausmeister des Genoms‘ (‚Caretaker of the Genome‘) bezeichnet“, beschreibt Aswin Mangerich dessen grundlegende Funktion.
Dr. Arthur Fischbach, der an dem Projekt im Rahmen seiner inzwischen abgeschlossenen Doktorarbeit maßgeblich beteiligt war, berichtet weiter: „Das Enzym PARP-1 erkennt DNA-Schäden, wird dadurch aktiviert und bildet das Biopolymer Poly(ADP-Ribose) als eine der ersten Reaktionen der Zelle. Das Biopolymer bewirkt wiederum über eine sogenannte nicht-kovalente (lockere) Ankopplung anschließend eine kovalente (feste) Ankopplung an p53. Diese Modifikation hat weitreichende Auswirkungen für die Regulierung der biochemischen und zellulären Funktionen von p53.“
Der „Wächter“ und der „Hausmeister“ des Genoms tun sich somit zusammen, wobei es der Hausmeister ist, der bei einer Gefährdung der Zelle den Wächter ruft und anweist. Die Forschung wurde finanziell unterstützt von der Deutschen Forschungsgemeinschaft (DFG), vom Sonderforschungsbereich SFB 969 „Chemical and Biological Principles of Cellular Proteostasis“ sowie von der Graduiertenschule Chemische Biologie und dem Zukunftskolleg der Universität Konstanz, die im Rahmen der Exzellenzinitiative des Bundes und der Länder gefördert werden.
Quelle: Universität Konstanz
Originalpublikation: A. Mangerich et al.; The C-terminal domain of p53 orchestrates the interplay between non-covalent and covalent poly(ADP-ribosyl)ation of p53 by PARP1; Nucleic Acids Research, 2018; doi: 10.1093/nar/gkx1205